Règlement (UE) 2023/607 : les étapes avant adoption
[article initialement publié le 2 février 2023]
Récapitulatif des étapes qui vont nous conduire au règlement (UE) 2023/607, visant à prolonger les périodes de transitions. Des liens sont fournis vers les documents associés.
- 2017-2022 : Les acteurs du DM alertent les autorités quant à l’insoutenabilité du calendrier du règlement.
- 14 juin 2022 : Des ministres évoquent les retards liés au RDM lors de la réunion du conseil EPSCO (9910/22, voir le résumé de la réunion). La commission rejette la faute aux fabricants.

- 10 octobre 2022 : Question à la commission soulevant les problèmes de disponibilité des dispositifs médicaux (O-000043/2022). Selon les procédures, cette question appelle obligatoirement une réponse d’ici au 11 janvier 2023.

- 6 décembre 2022 : Note d’information de la commission relative aux risques de pénuries remontés par les professionnels de santé (ST/15520/22)
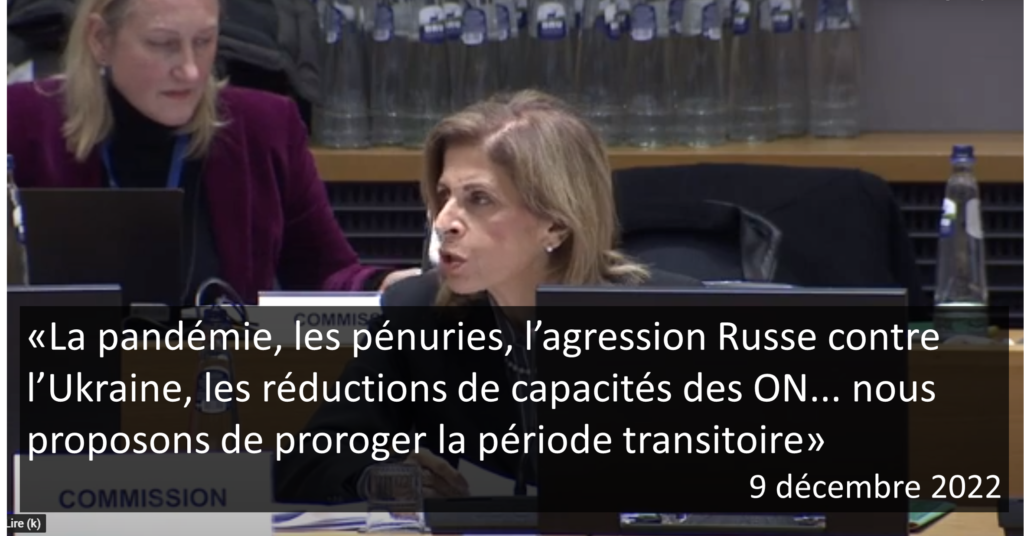
- 9 décembre 2022 : échanges avec les états membres au cours du conseil EPSCO (voir le résumé)
- 6 janvier 2023 : la commission soumet une proposition d’amendement au Conseil et au Parlement (COM/2023/10)
- 10 janvier 2023 : adoption par la commission
- 11 janvier 2023 : préparation de la discussion avec le conseil (ST/5139/23)
- 11 au 18 janvier 2023 : consultation publique (13684) [ci-dessous, un nuage des mots les plus utilisés dans les 246 commentaires reçus).

- 25 janvier 2023 : accord du Comité des représentants permanents (ST/5369/23).
- 26 janvier 2023 : proposition faite au parlement (ST/5585/23)
- 16 février 2023 : vote du parlement (séance plénière)
- 7 mars 2023 : approbation du conseil
- 20/03/2023 : adoption de l’amendement, publié au JOUE
Source : suivi de la procédure 2023/0005/COD
