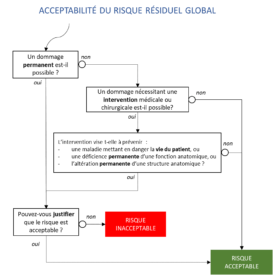
Article 61(10) MDR : l’approche de Team-NB et ses conséquences pour les fabricants
Article 61(10) MDR : dans quels cas un fabricant peut justifier une démonstration de sécurité et de performance sans données cliniques directes ? Décryptage de l’approche Team-NB.