MDCG Guidance on Periodic Safety Update Report, draft
Nouveau draft pour le guide MDCG relatif au PSUR et les annexes associées.
Pour rappel, le PSUR est obligatoire dès la classe IIa, il fait la synthèse de TOUS les éléments relatifs à la sécurité et aux performance de vos dispositifs, ces données sont issues de vos activités de SAC : études de SCAC, vigilance, suivi de l’état de l’art…
Grosse contrainte : ce document doit être lu de façon autonome, aussi vous devrez faire de nombreuses reprises de votre documentation technique et de vos enregistrements, ce qui peut facilement devenir laborieux.
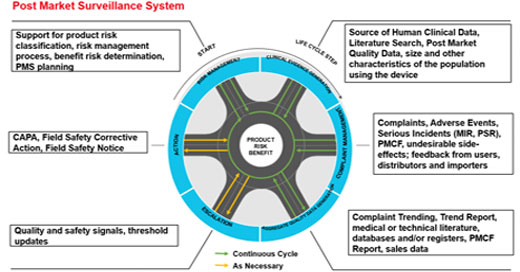
Contenu attendu
Le plan du rapport et le détail du contenu ne sont pas encore figés, mais cela devrait tourner autour d’une dizaine de rubriques :
- Résumé opérationnel : les principales informations sur le PSUR précédent et un résumé des données et résultats du PSUR courant.
- Description du dispositif et de son utilisation prévue
- Justification en cas de regroupement de plusieurs dispositifs (différents IUD-ID) dans un même PSUR, à justifier après analyse des avantages et inconvénients)
- Données quantitatives relatives aux ventes et aux utilisateurs
- Données de SAC
- Incidents graves
- Incidents non-graves
- FSCAs
- CAPAs
- Retours, plaintes
- Modification de l’état de l’art
- …
- Données de SCAC
- Études de SCAC
- Recherche dans la littérature
- Exploitation des registres
- Exploitation de données relatives à d’autres dispositifs
- Description et analyse des résultats
- Résumé
- Évaluation de la qualité (couverture, biais…)
- Comparaison avec les résultats antérieurs
- Comparaison avec d’autres dispositifs
- Compatibilité des résultats
- Description des signaux et de leur analyse
- Réévaluation du rapport bénéfice risque
- (Ré)estimation des bénéfices confirmés, nouveaux, non-atteints
- (Ré)estimation des bénéfices confirmés, nouveaux, non-atteints
- Réévaluation de la balance B/R
- Conclusion
- Déclaration sur l’évolution du rapport B/R
- Incertitudes
- Nouveaux / mise à jour des objectifs de surveillance
Il est demandé d’utiliser la terminologie IMDRF sur les effets indésirables pour la présentation des données et des résultats.
Un travail conséquent, pour réconcilier votre documentation technique avec le monde réel
Les exigences en matière de PSUR sont très orientées vigilance, l’idée est de confronter les résultats de vos évaluations (cliniques, risques, IAU, techniques) avec la réalité du terrain, de passer d’une DT conforme à la conformité des faits.
Attention, rédiger un PSUR demande un gros travail, il est conseillé de l’alimenter en continu, avec les données de sortie de vos activités de surveillance et vigilance.
