Proposition d’amendement au règlement 2017/745 pour rallonger les périodes de transitions
Suite à la réunion EPSCO du 9 décembre 2022, un amendement au RDM est proposé pour prolonger les périodes de transition.Il doit maintenant être adopté par le Parlement et le Conseil de l’UE.
La commission résume la situation dans un communiqué de presse, une FAQ et une factsheet.
Le document 2023/0005 porte l’amendement.
Modification de l’article 120 du règlement (dispositions transitoires)
L’article 120 fixe les modalités de la période de transition pour les dispositifs déjà CE selon une directive (DM ou DMIA). Avec l’amendement, les dates de fin de la période de transition sont largement rallongées :
- 26 mai 2026 pour les classes III implantables sur mesure ;
- 31 décembre 2027 pour les classes III et IIb implantables hors sutures, agrafes, produits d’obturation dentaire, appareils orthodontiques, couronnes dentaires, vis, cales, plaques, guides, broches, clips et dispositifs de connexion ;
- 31 décembre 2028 pour les autres DM impliquant un organisme notifié pour le règlement
Pour limiter les risques de pénurie, l’amendement souhaite supprimer la limite de date de mise à disposition sur le marché ou de mise en service, précédemment fixée au 26 mai 2025 (article 120.4).
Quelle date limite pour mettre sur le marché les DM CE selon une directive ?
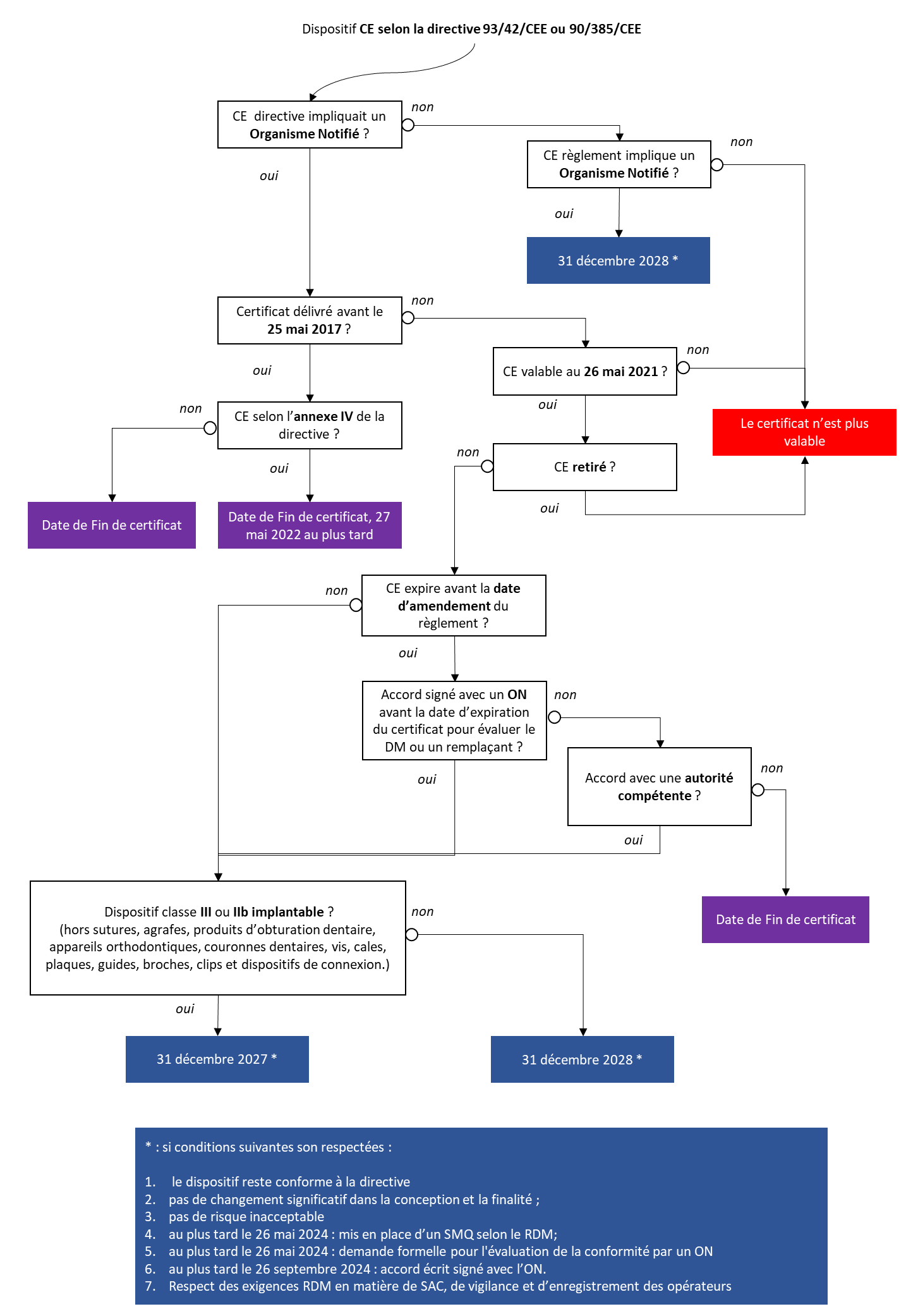
Cas des DM classe III implantables sur mesure

Analyse des causes
Pour l’histoire, notez que les causes justifiant ce report varient d’une source à l’autre :
- Commissaire européenne à la santé : Crise Covid-19, Crise des matières premières, Guerre en Ukraine, Incapacité des Organismes Notifiés
- FAQ de la commission : Incapacité des Organismes Notifiés, Mauvaise préparation des fabricants
- Factsheet de la commission : Incapacité des Organismes Notifiés, Mauvaise préparation des opérateurs économiques
Sans jamais remettre en question la surenchère réglementaire ni la mauvaise préparation de l’UE (Eudamed, normes harmonisées, spécifications communes…)
Source : Commission Européenne

5 commentaires