Distributeurs : obligations avec le règlement dispositifs médicaux
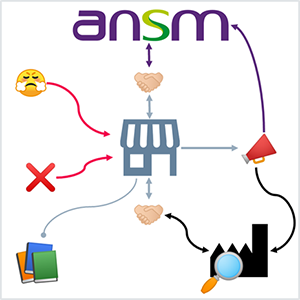
Qu’ils soient spécialisés ou généralistes, petits ou gros, en ligne ou physiques : les distributeurs de dispositifs médicaux voient leurs obligations considérablement augmenter avec le nouveau règlement 2017/745 relatif aux dispositifs médicaux.
Tour d’horizon des exigences applicables aux distributeurs, du contrôle des produits à la gestion des actions de matériovigilance.
📑 Avant propos : le distributeur dans le règlement
- Définition de distributeur
- Article 14 : obligations générales pour les distributeurs
La définition est la suivante :
toute personne physique ou morale faisant partie de la chaîne d’approvisionnement, autre que le fabricant ou l’importateur, qui met un dispositif à disposition sur le marché, jusqu’au stade de sa mise en service
Il est important de comprendre que le distributeur n’est généralement pas unique, on prendra en compte toute la chaîne de distribution allant du fabricant à l’utilisateur, de même le distributeur n’est pas forcément en contact direct avec le client final.
🔍 Vérification des dispositifs et des documents fournis
Le distributeur doit vérifier la conformité des produits qu’il met à disposition ainsi que le respect par le fabricant de certaines démarches réglementaires :
🗸 Le dispositif porte le marquage CE
🗸 Une déclaration de conformité UE a été établie par le fabricant
🗸 La notice d’utilisation et l’étiquetage sont conformes aux exigences du règlement (voir annexe I chapitre III sur les informations fournies à l’utilisateur)
🗸 L’ IUD (Identifiant Unique du Dispositif) a bien été attribué par le fabricant
🗸 Pour les dispositifs importés : l’importateur s’est clairement identifié sur le dispositif et/ou les documents d’accompagnement
🗸 Les conditions de stockage et de transport sont spécifiées et le distributeur est en mesure de les respecter
Le travail de vérification est très conséquent, impossible de vérifier de façon exhaustive la conformité des produits et l’ensemble des documents fournis, il est probable que cela se limite à un contrôle de la présence des informations et de quelques points critiques (ex : coordonnées du fabricant, contre-indications, …).
À noter : le règlement offre la possibilité de travailler par échantillonnage, il n’est donc pas question de contrôle chaque dispositif avant distribution.
📚 Tenue de registres et traçabilité
“Les paroles s’envolent, les écrits restent”
Le distributeur est tenu de tenir des registres pour enregistrer les événements suivants :
- Non-conformités des dispositifs
- Réclamations des utilisateurs
- Rappels par le fabricant
- Retraits par le fabricant
Ces registres seront évidement consultables, sur demande, par l’autorité compétente (l’ANSM en France).
Le distributeur doit mettre en place une traçabilité des dispositifs mis à disposition, pour – le cas échéant – pouvoir collaborer avec le fabricant lors des actions de surveillance et de vigilance :
“Les distributeurs et les importateurs coopèrent avec les fabricants ou leur mandataire pour atteindre un niveau approprié de traçabilité des dispositifs.”
article 25
❌ Gestion des dispositifs Non-Conformes
Le distributeur est tenu d’agir en cas de (soupçon de) dispositif non-conforme aux exigences de sécurité et de performances, principalement.
Deux cas, selon si la détection de la N.C. se fait avant ou après mise à disposition :
- Détection de la N.C. avant mise à disposition :
- Informer le fabricant
- Lorsqu’applicable : informer le mandataire et l’importateur
- Ne pas distribuer le dispositif avant correction de la non-conformité
- Détection de la N.C. après mise à disposition (DM utilisé) :
- Informer immédiatement le fabricant
- Le cas échéant : informer immédiatement mandataire et importateur
Le traitement des non-conformités est sous la responsabilité du fabricant, le distributeur doit le prévenir et mettre en œuvre les actions correctives éventuelles.
📢 Information des autorités en cas de risque grave ou de DM falsifié
Et le distributeur devient un acteur majeur de la vigilance :
- En cas de (soupçons de) dispositif falsifié : le distributeur prévient l’autorité compétente
- En cas de (soupçons de) dispositif présentant un risque grave : le distributeur prévient les autorités compétentes des pays dans lesquels il a mis le DM à disposition, il précise les cas constatés de NC ainsi que les mesures correctives qui ont été prises
Deux notions sont à préciser pour comprendre ces exigences :
dispositif falsifié
Tout dispositif comportant une fausse présentation de son identité et/ou de sa source et/ou de ses certificats de marquage CE ou des documents relatifs aux procédures de marquage CE. La présente définition n’inclut pas les cas de non-respect non intentionnels et s’entend sans préjudice des violations des droits de propriété intellectuelle
Risque grave n’est pas défini, mais on considère qu’il peut conduire à un incident grave :
incident grave
Tout incident ayant entraîné directement ou indirectement, susceptible d’avoir entraîné ou susceptible d’entraîner:
a) la mort d’un patient, d’un utilisateur ou de toute autre personne;
b) une grave dégradation, temporaire ou permanente, de l’état de santé d’un patient, d’un utilisateur ou de toute autre personne;
c) une menace grave pour la santé publique;
😤 Réclamations et signalements
Le distributeur est classiquement la première interface d’un utilisateur en cas de problème, c’est à lui de remonter au fabricant ces informations d’après commercialisation. Lorsqu’applicable le mandataire et l’importateur sont également prévenus.
Réclamation et signalement ne sont pas définis par le règlement, on retiendra les implications suivantes :
- Réclamation : une remontée d’information liée à un mécontentement de l’utilisateur, l’important est de comprendre si la réclamation porte sur une non-conformité (du dispositif, des documents, des prestations associées, …); sur des problèmes d’usage (mauvaise aptitude à l’utilisation) ou sur des points ne remettant pas en cause la conformité du DM (comme des pistes d’amélioration ou des remarques d’ordre commercial)
- Signalement : l’utilisateur remonte une non-conformité ou un incident avéré
🤝 Coopération avec les autorités et le fabricant
Plusieurs situations impliquent la coopération des distributeurs pour les actions de vigilance et de mise en conformité :
- Mise en œuvre des mesures correctives face à une N.C., un rappel ou un retrait. En coopération avec le fabricant, son mandataire, son distributeur et l’autorité compétente.
Et à la demande de l’autorité compétente :
- communication des informations et des documents prouvant la conformité d’un dispositif
- fourniture d’échantillon gratuit ou possibilité d’accès à un dispositif
- mise en œuvre de mesure décidée par l’autorité compétente pour éliminer un risque
Conclusion
L’intention du règlement est claire : consolider la surveillance après commercialisation, les distributeurs sont logiquement mis à contribution.
D’ici la mise en application du règlement en mai 2020 (voir le calendrier détaillé) les distributeurs vont devoir s’organiser pour répondre aux exigences, avec des procédures permettant de contrôler les dispositifs, vérifier les informations fournies, communiquer avec les opérateurs économiques et les autorités compétentes, gérer les dispositifs non-conformes, … de quoi créer un véritable système de management de la qualité, en accord avec l’ISO 13485:2016 qui s’ouvre à tous les acteurs du DM.

37 commentaires