Résumé de la norme IEC 82304-1 : Logiciels de santé

Résumé des exigences de la norme IEC 82304-1:2016 “Logiciels de santé Partie 1 : Exigences générales pour la sécurité des produits”.
Applicable aux logiciels de santé en général elle est de plus en plus exigée par les organismes notifiés pour la documentation technique des logiciels dispositifs médicaux, elle comble en effet un vide dans le contexte normatif actuel, notamment en matière de validation.
IEC 82304-1, la norme des logiciels de santé
L’IEC 82304-1 est destinée aux produits logiciels de santé, c’est-à-dire le logiciel de santé et les documents d’accompagnement associés.
La notion de santé est vaste et englobe le médical : des milliers de logiciels sont ainsi concernés.
La norme décrit les activités à mettre en place pour garantir la sécurité, elle couvre tout le cycle de vie : de la conception à la mise hors service, en passant par la validation et la maintenance.
La norme ne s’applique pas aux logiciels embarqués
Les dispositifs électromédicaux ne sont pas concernés par la norme, leur sécurité étant déjà démontrée via l’IEC 62304 (décrivant le cycle de vie des logiciels (de) dispositif médicaux) et les autres normes applicables : IEC 60601, IEC 61010 ou ISO 14708.
Contexte règlementaire et normatif
Utilisation de l’IEC 82304-1 à des fins règlementaires
La norme entre dans le champ d’application du règlement (UE) 2017/745.
La date de dow (date limite de mise en œuvre d’une norme, les précédents standards n’étant plus reconnus) est fixée au 1er septembre 2020. Mais dans les faits elle est déjà exigée lors des audits, il semble nécessaire de la mettre en œuvre dès maintenant.
IEC 82304-1 et IEC 62304
L’IEC 62304 est directement appelée par l’IEC 82304-1, notez que dans le cas des applications de santé non médicales le vocabulaire doit être adapté :
- Médical ⇨ Santé
- Patient ⇨ Utilisateur
Actuellement en cours de révision la prochaine version de la 62304 sera étendue à tous les logiciels de santé (vraisemblablement en 2019).
Le tableau suivant indique les normes à prendre en compte selon que le logiciel soit embarqué ou autonome, avec une finalité santé ou médicale :
| Dispositif de Santé | Dispositif Médical | |
|---|---|---|
| Logiciel Embarqué | IEC 62304 (révision 2019) | IEC 62304 + IEC 60601-1 |
| Logiciel Autonome | IEC 82304-1 + IEC 62304 | IEC 62304 + IEC 82304-1 |
IEC 82304-1 et autres normes applicables à un DM logiciel autonome
Les normes applicables sont reportées ci-dessous en regard du cycle de vie d’un logiciel médical :
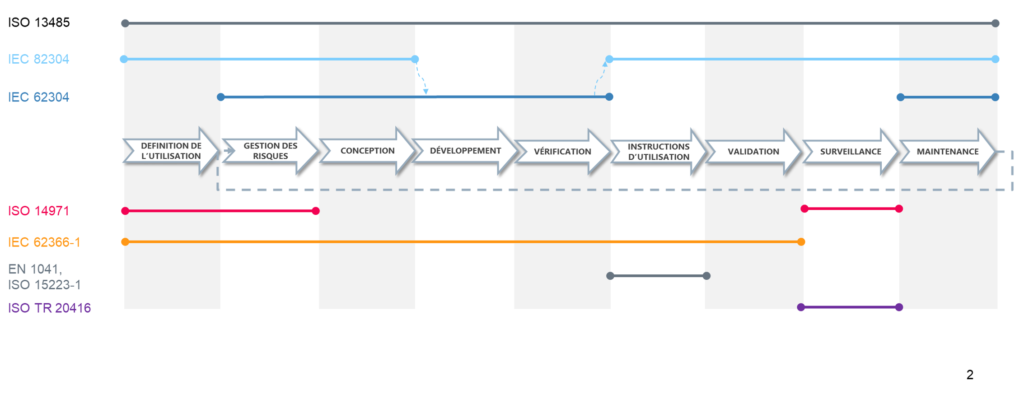
(la suite de l’article reprend les titres des chapitres de l’IEC 82304-1)
Termes et définitions
Voir les définitions sur le site de l’ISO, elles sont souvent issues de normes médicales.
On notera la définition de “logiciel de santé” (et l’absence de définition de “santé” :( ).
Exigences concernant les produits logiciels de santé
Les exigences visent à définir l’emploi prévu; l’interface utilisateur; les exigences de sécurité, d’immunité et de protection des données personnelles; ainsi que les instructions fournies à l’utilisateur; tout en tenant compte du contexte règlementaire. Les risques sont maitrisés, les exigences seront vérifiées, les modifications sont gérées.
Rien de bien nouveau en contexte DM.
Néanmoins, des précisions (comme sur les exigences systèmes) sont à prendre en compte.
Processus du cycle de vie du logiciel
La norme renvoi aux § 4 à 9 de l’IEC 62304 (exigences générales, développement, maintenance, gestion des risques, gestion de configuration et gestion de problème (!) ).
Ces deux normes vont ainsi devenir vos livres de chevet.
Templates pour la mise en œuvre de l’IEC 62304
Validation des produits logiciels de santé
Les validations sont demandées par la règlementation DM et l’ISO 13485, pour les logiciels autonomes la 82304-1 comble ici un vide.
Pour valider un logiciel, il faudra :
- Planifier la validation, dans un plan qui identifie le domaine d’application, évalue les limites des activités de validation (qui ne sont jamais parfaitement exhaustives), définit les critères et méthodes nécessaires.
- Justifier l’indépendance des personnes impliquées dans la validation
- Rédiger un rapport de validation en tenant compte des résultats, des écarts et du risque résiduel
Identification des produits logiciels de santé et Documents d’accompagnement
Identification
Le logiciel est identifié de manière unique en appliquant la règlementation (voir l’IUD demandé par le règlement DM), ce dans un souci de traçabilité.
Documents d’accompagnement
Les instructions d’utilisation incluent :
- une description de l’environnement informatique d’utilisation (notamment réseau);
- les avertissements et consignes de sécurité;
- une explication des messages utilisés dans le logiciel
- une explication des procédures spéciales, lorsqu’ applicable: installation, démarrage, arrêt ou mise hors service.
Une description technique est exigée, elle inclue notamment :
- les exigences sur le système dans lequel est utilisé le logiciel
- les caractéristiques et performances (précision, plages, erreurs…)
- les informations nécessaires pour comprendre et mettre en œuvre les réglages impactant la sureté technique (et donc les performances)
- toutes les informations nécessaires en cas de connexion à un réseau : caractéristiques, flux d’information, modifications apportées au réseau…
Activités d’après commercialisation
- Les activités de maintenance doivent être maitrisées (analyse d’impact, analyse des risques, enregistrements, essais…) et entrainer une nouvelle validation.
- Le fabricant doit communiquer au près des utilisateurs et des autorités en cas :
- de problème de sureté ou de sécurité, même en cas de vulnérabilité qui n’a pas encore donné lieu à un incident
- de mise à jour du logiciel ou des documents fournis
Enfin, la maitrise de la mise hors service du dispositif est un impératif.
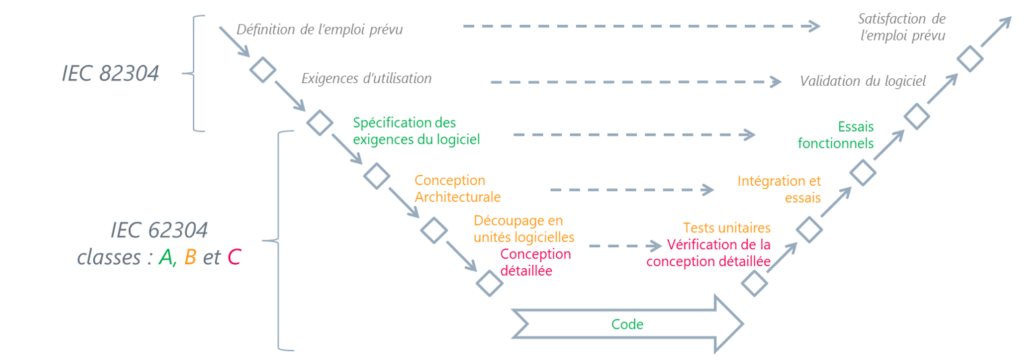
Cycle en V
Ce schéma complète le cycle en V de l’IEC 62304 avec les exigences de l’IEC 82304 :