Principaux textes règlementaires Européens pour les dispositifs médicaux et de santé

Pour un fabricant l’identification des règlementations Européennes applicables à un produit est la première étape en vue de l’obtention du marquage CE obligatoire pour une commercialisation dans l’UE.
Cet article fait le tour des textes dédiés aux dispositifs médicaux (DM) et de ceux plus généraux mais néanmoins applicables : dispositifs électroniques, machines, stockage des données personnelles, piles et accumulateur… D’autres sont cités uniquement pour info.
Une liste d’objectifs, centrés sur un secteur économique / une industrie, définis par la commission Européenne et appliquée par les États membres.
À définir un cadre commun pour mettre sur le marché de l’UE des produits sûrs et performants.
Une directive est adaptée dans le droit national, un règlement est appliqué en l’état.
2 règlements : 2017/745/UE et 2017/746/UE pour les DM et les DM-DIV.
Oui, si les exigences ne sont pas déjà couvertes. Par exemple les directives RED ou RoHS sont applicables aux dispositifs médicaux.
Règlementation Européenne et marquage CE – Introduction
Définitions
Une Directive Européenne est un acte juridique défini par la commission Européenne fixant des objectifs pour les États membres qui les transposent dans leur droit national. Chaque état est libre de choisir les moyens pour atteindre les objectifs définis dans les directives.
Un Règlement Européen est un acte juridique qui revêt une portée générale, il est obligatoire dans tous ses éléments et est il appliqué immédiatement en tant que norme dans l’ensemble des pays de l’UE sans devoir être transposé dans le droit national.
Utilité
Une règlementation Européenne définit des exigences à respecter pour pouvoir apposer le marquage CE sur un produit qui sera alors librement commercialisable dans tous les pays de l’Union Européenne. Ces exigences concernent le plus souvent les performances et la sécurité mais aussi le marquage, les instructions d’utilisations associées… Des exigences peuvent également impacter les activités du fabricant comme la mise en place d’un système de management de la qualité, de procédures de surveillance des produits, de communication avec les autorités nationales…
Portée
Le champ des textes règlementaires Européens est très vaste : du jouet à l’aéronautique en passant par les dispositifs médicaux le site de la commission Européenne propose un portail vers différents secteurs économiques, un espace “législation” est accessible pour chaque secteur.
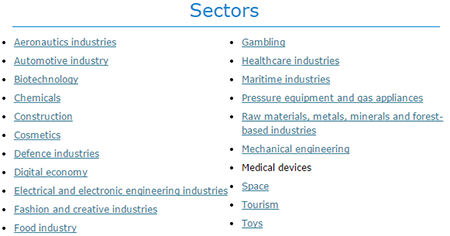
Versions consolidées
Les textes sont parfois proposés en version consolidée : une version où le texte d’origine a été mis à jour en fonction des modifications apportés par d’autres textes (des directives et des règlements publiés ultérieurement).
Références des textes règlementaires
La construction des références est faite de manière systématique :
Année / Numéro incrémental / Europe
Il est amusant de voir que la fin des références a évolué avec la construction de l’Union Européenne :
- CEE : Communauté Économique Européenne, fruit du traité de Rome (1957)
- CE : Communauté Européenne, suite au traité de Maastricht (1992)
- UE : Union Européenne, après le traité de Lisbonne (2007)
Remarque : année et N° sont parfois inversés.
Directives Européennes applicables aux DM (jusqu’en 2020)

3 directives concernent les DM : 93/42/CEE (la plus générale) 98/79/CE (DM de diagnostic in vitro) et 90/385/CE (DM implantables actifs).
Leur application est exclusive, par exemple un DMIA n’est pas concerné par la 93/42/CEE.
Directive 93/42/CEE relative aux dispositifs médicaux
La directive 93/42/CEE s’applique aux dispositifs médicaux et à leurs accessoires.
Pour savoir si elle est applicable il faut mettre en regard la définition d’un dispositif médical et la destination revendiquée par le fabricant.
Sont exclus du champ de la directive les dispositifs de diagnostic in vitro (DM-DIV) et les dispositifs médicaux implantables (DMIA), en Europe ces types de dispositifs médicaux ont leurs propres directives.
Cette directive est relativement détaillée, on y trouve notamment:
- Des définitions utiles (accessoire, données cliniques, fabricant…)
- La liste des exigences essentielles pour les dispositifs médicaux
- La mise en avant des normes harmonisées à la 93/42/CEE comme moyen de réponse aux exigences
- Les règles de classification des DM
- Les différentes procédures de marquage CE
- Des détails sur le rôle et la nature des organismes notifiés, des évaluations cliniques…
Directive 98/79/CE relative aux dispositifs médicaux de diagnostic in vitro
La directive 98/79/CE concerne les dispositifs médicaux de diagnostic in vitro et leurs accessoires, une définition est donnée dans l’article premier, les cas “borderline” peuvent être abordés à la lumière du guide MEDDEV 2.14/1.
La construction du document est proche de la 93/42/CEE : définitions, exigences essentielles, normes harmonisées, procédures d’évaluation de la conformité, surveillance du marché…
Directive 90/385/CEE relative aux dispositifs médicaux implantables actifs
La directive 90/385/CEE est propre aux dispositifs médicaux implantables actifs, le champ d’application est détaillé dans le guide MEDDEV 2.1/2.
Encore une fois comparable aux autres directives sur les DM: définitions, marquage CE, exigences essentielles…
Règlements Européens relatifs aux dispositifs médicaux (transition de 2017 à 2020)
Deux règlements vont remplacer les directives DM :
- Règlement (UE) 2017/45 relatif aux dispositifs médicaux (dont implantables actifs)
- Règlement (UE) 2017/746 relatif aux DM-DIV
La période de transition va aller jusqu’en 2020 (voir le planning).
À noter, le règlement (UE) 207/2012 relatif aux instructions d’emploi électroniques des dispositifs médicaux (applicable si vous ne fournissez pas d’instruction utilisateur en format papier).
Directives Européennes sur les dispositifs électriques et électroniques
Hormis la directive RED les directives suivantes ne sont pas applicables aux DM, car les exigences sont déjà couvertes par les directives “médicales”.
Ces textes s’appliquent aux dispositifs “grand public”, notamment de santé / bien-être.
Directive 2004/108/CE concernant la compatibilité électromagnétique
L’idée de la 2004/108/CE est que les dispositifs électroniques doivent assurer une compatibilité électromagnétique (CEM), ce qui induit :
- De ne pas perturber les autres dispositifs (contraintes en émission)
- De ne pas être perturbé par d’autres dispositifs (contraintes d’immunité)
Les dispositifs électroniques sont des sources de rayonnement électromagnétique, d’autant plus sévère qu’ils travaillent à des fréquences et/ou des puissances électriques élevées. Ces rayonnements sont susceptibles de perturber le fonctionnement d’autres dispositifs en véhiculant des perturbations par onde radio, sur le réseau électrique, par les interconnexions…
Un bon exemple est le bruit d’un haut-parleur avec un téléphone portable actif à proximité : les ondes du mobile viennent parasiter votre système audio. Ce phénomène peut être nettement plus gênant lorsque le vérin d’un lit médicalisé vient parasiter le pacemaker du patient…
Avant d’apposer le marquage CE à un équipement le fabricant doit garantir le respect du produit aux exigences essentielles, cela passe par des essais selon des normes harmonisées (voir la liste) et le recours optionnel à un organisme notifié pour évaluer la conformité de la documentation technique qui a été constituée.
Des exigences complémentaires sont propres au marquage du produit et aux informations fournies à l’utilisateur.
Directive 2014/35/UE dite “Basses Tensions”
La 2014/35/UE s’applique aux appareils fonctionnant entre 50 et 1000 Vac (courant alternatif) ou entre 75 et 1500 Vdc (courant continu), les appareils reliés au réseau domestique sont donc concernés.
La directive fixe des objectifs de sécurité d’utilisation, le fabricant pourra établir une déclaration CE de conformité après avoir testé son appareil selon les normes harmonisées applicables (voir la liste).
Des produits très spécifiques sont exclus du champ d’application de la directive : équipement destiné à une atmosphère explosive, compteur électrique, prise de courant domestiques… et les “matériels d’électroradiologie et d’électricité médicale“. A noter que les dispositifs médicaux ont leurs propres exigences en matières de sécurité électrique, la conformité peut être démontrée selon la norme IEC 60601-1.
Directive Européenne 2014/53/CE dite “RED”
RED pour Directive sur les Équipements Radioélectriques.
La directive 2014/53/CE concerne les dispositifs utilisant une communication hertzienne (radio) et/ou connecté à un réseau public de télécommunication.
Cette directive est applicable aux dispositifs médicaux (ils ne font pas partie des dispositifs exclus en annexe I).
Ici aussi on retrouve des exigences essentielles, la mise en conformité via des normes harmonisées, les procédures d’évaluation de la conformité…
Principaux autres textes règlementaires
La liste n’est pas exhaustive, mais ce sont des textes que l’on rencontre fréquemment :
- 2016/679 règlement relatif aux données à caractère personnel, applicable notamment dans le cadre d’un projet de santé connectée (voir la réglementation en e-santé).
- 2006/42/CE directive relative aux machines, ici une machine est un dispositif ayant des pièces en mouvement entraînées par autre chose qu’un animal (humain compris).
- 2016/425 règlement relatif aux équipements de protections individuels (EPI) : des dispositifs tenus ou portés par une personne pour protéger sa santé.
- 2014/31/UE relative aux Instruments de Pesage à Fonctionnement Non Automatique (IPFNA), les pèse-personnes utilisés à des fins médicales sont concernés par cette directive.
- 2011/65/UE dite “RoHS 2” relative à la limitation de l’utilisation de certaines substances dangereuses dans les équipements électriques et électroniques
- 2012/19/UE relative aux déchets d’équipements électriques et électroniques (DEEE)
- 94/62/CE relative aux emballages et aux déchets d’emballages
- 80/181/CEE concernant le rapprochement des législations des États membres relatives aux unités de mesure
- 2006/66/CE relative aux piles et accumulateurs ainsi qu’aux déchets de piles et d’accumulateurs
- 2009/125/CE établissant un cadre pour la fixation d’exigences en matière d’écoconception applicables aux produits liés à l’énergie
- 2001/83/CE instituant un code communautaire relatif aux médicaments à usage humain, cette directive peut être utile pour définir si un DM incorpore un médicament (est devient un DM de classe III)
- 2001/95/CE relative à la sécurité générale des produits

4 commentaires